|
酸、碱稀释后溶液pH值的计算(选修4)<-->盐类水解网络图
溶度积常数(选修4)
〖定义〗
在一定条件下,难溶强电解质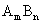 溶于水形成饱和溶液时,溶质的离子与该固态物质之间建立动态平衡,叫做沉淀溶解平衡。这时,离子浓度的乘积为一常数,叫做溶度积常数,简称溶度积,符号为 溶于水形成饱和溶液时,溶质的离子与该固态物质之间建立动态平衡,叫做沉淀溶解平衡。这时,离子浓度的乘积为一常数,叫做溶度积常数,简称溶度积,符号为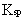 。 。
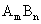  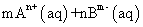 , ,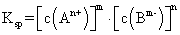
〖影响因素〗
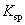 只与难溶电解质的性质和温度有关,与沉淀的量和溶液中离子的浓度无关。 只与难溶电解质的性质和温度有关,与沉淀的量和溶液中离子的浓度无关。
〖判断沉淀能否生成的依据〗
通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积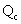 的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解。 的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解。
①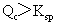 溶液过饱和,有沉淀析出,直至溶液饱和,达到以新的平衡。 溶液过饱和,有沉淀析出,直至溶液饱和,达到以新的平衡。
②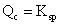 溶液饱和,沉淀与溶解处于平衡状态。 溶液饱和,沉淀与溶解处于平衡状态。
③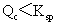 溶液未饱和,无沉淀析出。 溶液未饱和,无沉淀析出。
〖意义〗
溶度积反映了物质在水中的溶解能力。对于阴阳离子个数比相同的电解质,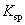 数值越大,电解质在水中的溶解能力越强;对于阴阳离子个数比不同的电解质,不能直接比较 数值越大,电解质在水中的溶解能力越强;对于阴阳离子个数比不同的电解质,不能直接比较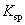 的数值大小,而确定其溶解能力的大小,需转化为溶解度来比较。 的数值大小,而确定其溶解能力的大小,需转化为溶解度来比较。
酸、碱稀释后溶液pH值的计算(选修4)<-->盐类水解网络图
全网搜索"溶度积常数(选修4)"相关
|

